Ley de BOYLE (Presión y Volumen) YouTube

Química Ley de Boyle. La ley de Boyle fue descubierta por Robert Boyle en el siglo XVII, y fue la ley que estableció las bases para poder explicar la relación que existe entre la presión y el volumen que existe en un gas.Por medio de una serie de experimentos, logró demostrar que, si había una temperatura constante, un gas al ser sometido a más presión reduce su volumen, mientras que.
PPT LEYES DE LOS GASES PowerPoint Presentation, free download ID447196

P₁ * V₁ = P₂ * V₂. (2 atm) * (10 L) = (4 atm) * V₂. 20 L atm = 4 atm * V₂. Dividiendo ambos lados de la ecuación por 4 atm: (20 L atm) / (4 atm) = V₂. V₂ = 5 L. Por lo tanto, el nuevo volumen del gas será de 5 litros cuando la presión aumente a 4 atmósferas. La ley de Boyle-Mariotte es una ley química que establece una.
Dato Químico Ley de Boyle

👀👨🎓 Les dejo el procedimiento para despejar las variables de la Fórmula de La Ley de Boyle-Mariotte. Espero que sea comprensible, te guste y sobre todo q.
Temas Selectos de Química Ley de los gases

Ley de Boyle-Mariotte. La ley de Boyle Mariotte ( ley de Boyle) es una de las leyes de los gases que relaciona el volumen y la presión de una cierta cantidad de gas mantenida a temperatura constante. La ley de Boyle-Mariotte fue formulada independientemente por el físico y químico irlandés Robert Boyle en 1662 y el físico y botánico.
Ecuación de los gases Academia Alfa10

Podemos escribir la ecuación de la ley de Boyle de la siguiente manera: p 1 × V 1 = p 2 × V 2,. donde p 1 y V 1 son la presión y el volumen iniciales, respectivamente. Del mismo modo, p 2 y V 2 son los valores finales de estos parámetros del gas. Podemos escribir la fórmula de la ley de Boyle de otras formas dependiendo del parámetro que queramos estimar.
Ley de Boyle Mariotte YouTube

⛳ La ley de Boyle describe la relación entre la presión y el volumen cuando T y n son constantes Ecuación P1V1=P2V2 ⛳ ejemplos resueltos y más
Ley de Boyle establece la presión de un gas Química Wikisabio

9.7: Ley de Boyle. Probablemente ya estés familiarizado con el hecho de que cuando exprimes un gas, ocupará menos espacio. En términos formales, aumentar la presión sobre un gas disminuirá su volumen. El científico inglés Robert Boyle estudió este fenómeno y finalmente se le ocurrió la Ley de Boyle como resultado.
Ley de Boyle

En 1662, Boyle publicó la primera ley física que venía dada en forma de ecuación, la cual señalaba la dependencia funcional de dos variables. En este caso, la presión y el volumen. Boyle señaló que existía una relación inversa entre la presión ejercida sobre un gas y el volumen que ocupaba ese gas, siendo esta relación relativamente cierta para los gases reales.
Cómo utilizar la fórmula de la ley de Boyle para gases ideales YuBrain
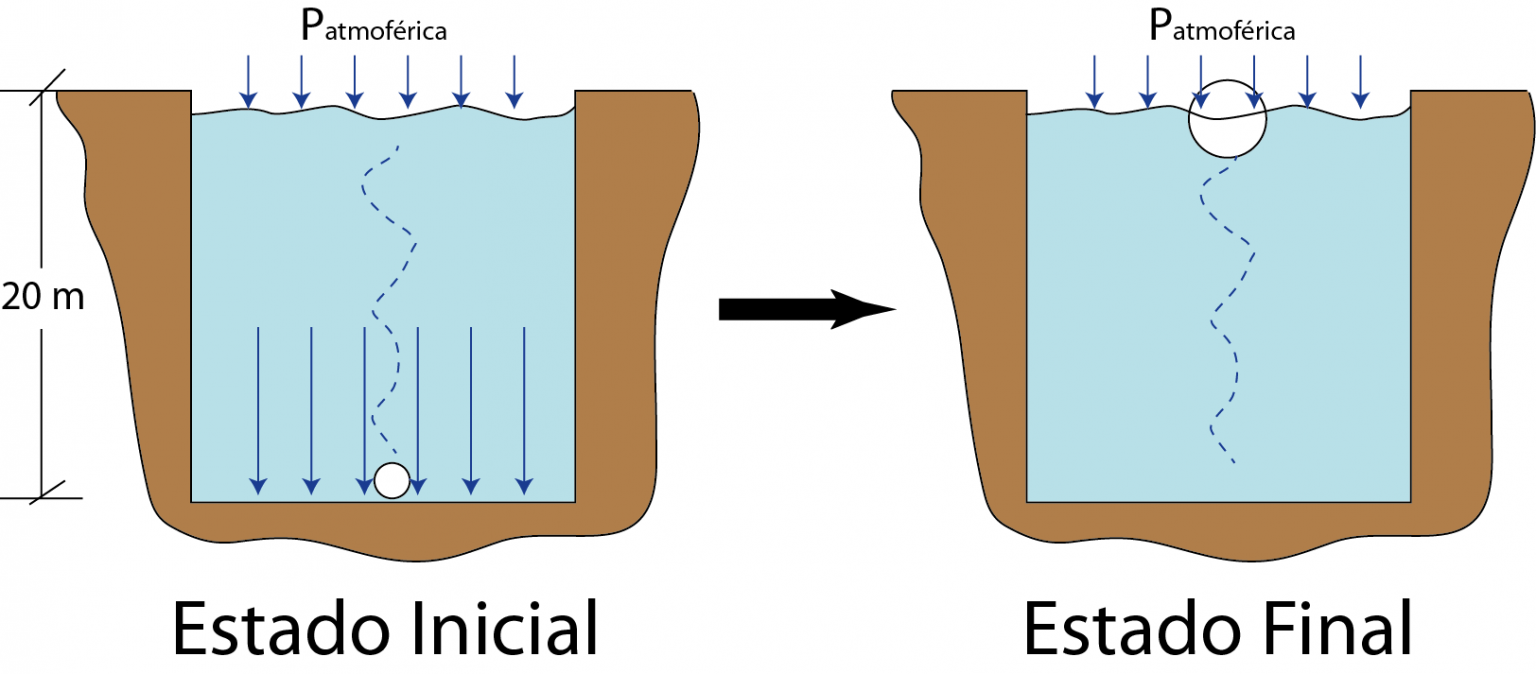
Figura 14.3.1: Robert Boyle. (CC POR-NC; CK-12) Matemáticamente, la ley de Boyle se puede expresar por la ecuación: P × V = k. El k es una constante para una muestra dada de gas y depende únicamente de la masa del gas y de la temperatura. La siguiente tabla muestra los datos de presión y volumen para una cantidad establecida de gas a.
Ley de Boyle Explicación y Ejemplo YouTube

2.1: Ley de Boyle. Robert Boyle descubrió la ley de Boyle en 1662. El descubrimiento de Boyle fue que la presión, P, y el volumen, V, de un gas son inversamente proporcionales entre sí si la temperatura, T, se mantiene constante. Podemos imaginar redescubrir la ley de Boyle atrapando una muestra de gas en un tubo y luego midiendo su volumen.
Leyes de los gases Boyle y Charles YouTube

La ecuación matemática de la ley de Boyle es: = donde P indica la presión del sistema, V indica el volumen del gas, k es un valor constante representativo de la temperatura y el volumen del sistema.. Mientras la temperatura permanezca constante, la misma cantidad de energía que se le da al sistema persiste durante toda su operación y, por lo tanto, teóricamente, el valor de k.
Formulas de Fisica II Ley de Boyle

Solución. La clave en problemas como este es poder identificar qué cantidades representan qué variables a partir de la ecuación relevante. La forma en que está redactada la pregunta, deberías poder decir que 1.56 atm es P i, 7.02 L es V i, y 0.987 atm es P f.Lo que buscamos es el volumen final— V f.Por lo tanto, sustituyendo estos valores en P i V i = P f V f:
Ciencia y química.... y más química Leyes empiricas de los gases.

Matemáticamente hablando, la Ley de Boyle nos indica que si multiplicamos la presión por el volumen, ese valor será constante sin importar cuánto varíen esas dos magnitudes, siempre y cuando la temperatura se quede quieta (constante). Veamos un ejemplo de la Ley de Boyle. Supongamos que un cilindro contiene un volumen de 20L de un gas.
ley de Boyle YouTube

Pinicial Vinicial = Pfinal Vfinal (ECUACIÓN DE LEY DE BOYLE A UTILIZAR) 1) En un recipiente cerrado de 4 Litros se introduce Oxigeno hasta que este ejerce una Presión de 2 Atmósferas. Calcular la Presión que ejercerá el gas si reducimos el volumen hasta 2 Litros. 2) Tenemos Nitrógeno gaseoso en un recipiente de 0,8 Litros, ejerciendo una.
Química Ley de Boyle (relación entre presión y volumen) Enseñanza de química, Química

La calculadora de la Ley de Boyle para la presión final (`P_2 = (P_1*V_1)/V_2`) calcula la presión final (P2) de una cantidad fija de gas a una temperatura fija un cambio de estado desde una presión inicial (P1) y volumen (V1) hasta un volumen final (V2).
LeydeBoyle

b) el 1 P 1 P frente a V gráfico en la Figura 9.13. c) la ecuación de la ley de Boyle. Comente la exactitud probable de cada método. Solución (a) La estimación a partir del gráfico P-V da un valor de P en torno a 27 psi. (b) La estimación de la 1 P 1 P frente al gráfico V da un valor de unos 26 psi.
.